Кристаллическое строение металлов, Основы кристаллического строения металлов

Аллотропические видоизменения железа 4. Возможно также определение этих величин с помощью дифракции электронов и нейтронов. Наиболее тесное расположение атомов наблюдается в решетке гранецентрировнного куба. Кристаллическое строение металлов К атегория: Металлы Кристаллическое строение металлов Далее: Основные свойства металлов Все вещества в твердом состоянии имеют кристаллическое или аморфное строение. Рекристаллизация — процесс зарождения и роста новых зерен с меньшим количеством дефектов строения.
Существование одного и того же металла в нескольких кристаллических формах носит название аллотропии , или полиморфизма.
Температура при этих фазовых превращениях называется критической , а перестройка кристаллических форм — полиморфными превращениями. Основоположником изучения термических превращений в сталях сплавах «железо-углерод» был русский ученый Д. Им было открыто, что при нагреве твердой стали до определенных температур, зависящих от ее состава, в ней происходят внутренние превращения, приводящие к изменению свойств.
Открытие Д. Классификация металлов 6. Атомно-кристаллическое строение металлов с Основные типы кристаллических решеток металлов Элементарная ячейка объёмноцентрированной кубической ОЦК кристаллической решетки Элементарная ячейка гранецентрированной кубической ГЦК кристаллической решетки Элементарная ячейка гексагональной плотноупакованной ГПУ кристаллической решетки 7.
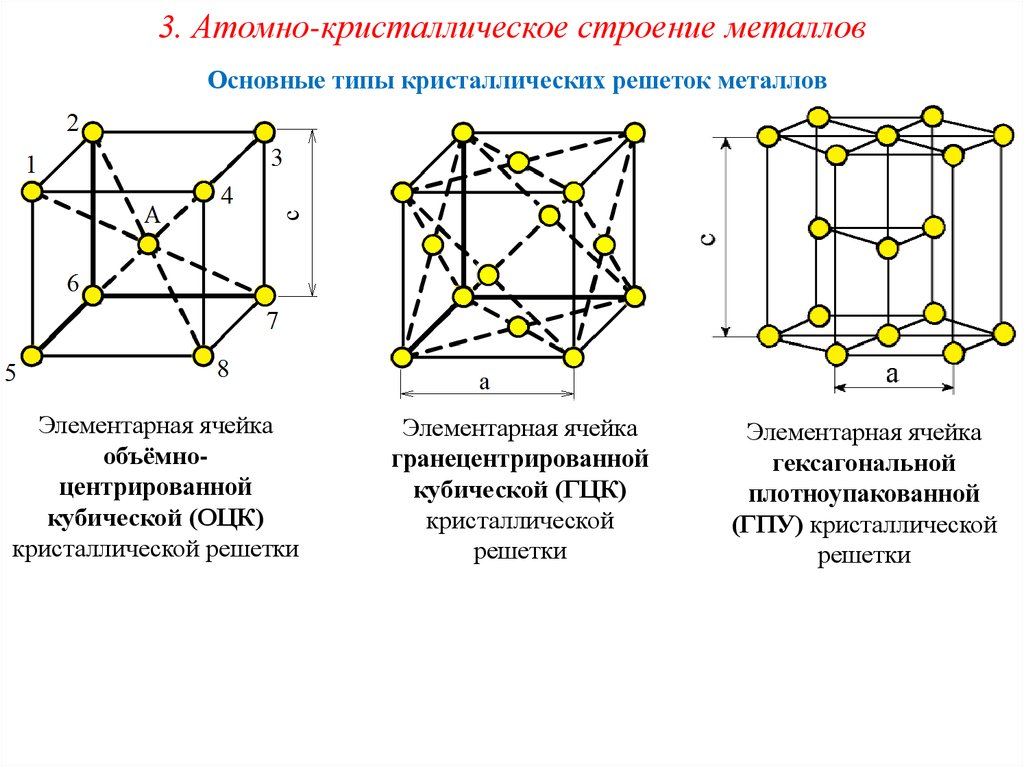
Атомно-кристаллическое строение металлов Характеристики кристаллических решеток с 1. Период параметр кристаллической решетки a, b, c — это расстояние между центрами ближайших атомов в элементарной ячейке. Коэффициент компактности плотность упаковки атомов — это отношение объема, занятого атомами, ко всему объему ячейки. Координационное число — это число атомов, находящихся на равном и наименьшем расстоянии от данного атома. Дефекты кристаллического строения металлов Дефекты кристаллического строения Точечные Линейные Поверхностные Объемные Дефекты кристаллического строения металлов Точечные дефекты 1.
Вакансия 3. Атом внедрения 2. Межузельный атом 4.

Атом замещения Дефекты кристаллического строения металлов Поверхностные дефекты Схема границы двух зёрен Объемные дефекты Трещины, поры, усадочные раковины и др. Все металлы и сплавы в твердом состоянии имеют кристаллическое строение.
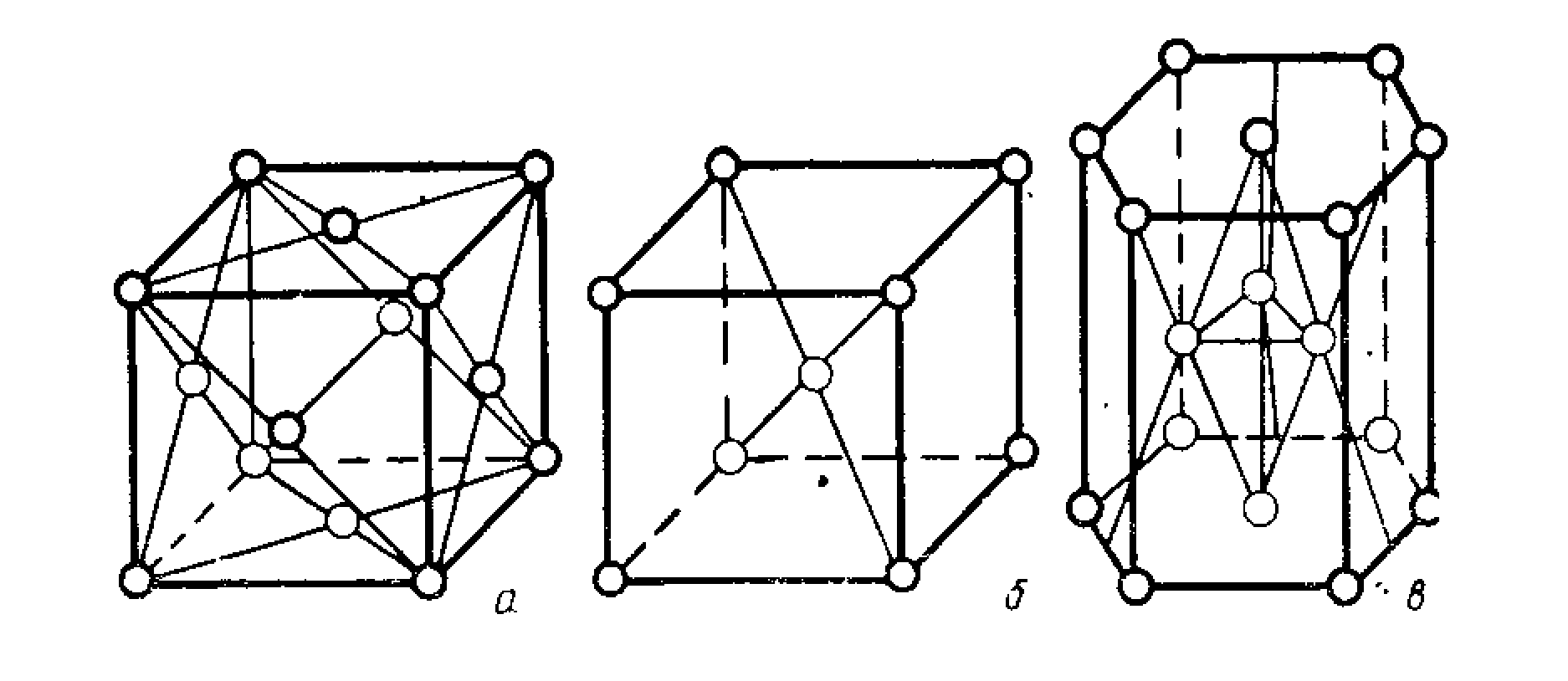
В отличие от некристаллических аморфных тел, у металлов атомы ионы расположены в строго геометрическом порядке, образуя пространственную кристаллическую решетку. Взаимное расположение атомов в пространстве и расстояния между ними устанавливаются рентгеноструктурным анализом. Для наглядного представления о расположении атомов в кристалле используют пространственные схемы в виде элементарных кристаллических ячеек. Наиболее распространенными типами кристаллических решеток являются кубическая объемноцентрированная, кубическая гранецентрированная и гексагональная.
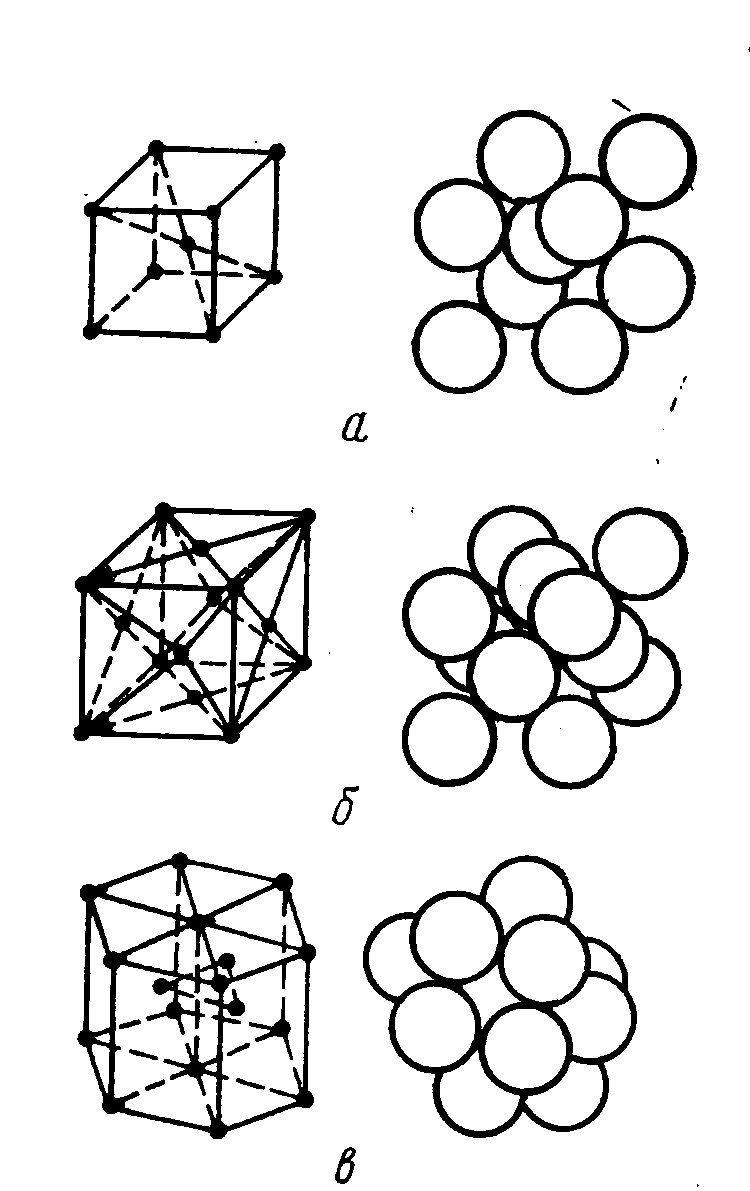
В кубической объемноцентрированной решетке расположено девять атомов. В кубической гранецентрированной решетке расположено 14 атомов. В гексагональной плотноупакованной решетке расположено 17 атомов. Такую решетку имеют: магний, цинк, кадмий и другие металлы. Взаимное расположение атомов в пространстве, количество атомов в решетке и междуатомные пространства характеризуют свойства металла электропроводность, теплопроводность, плавкость, пластичность и т.